Гемофилия
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
D66 – наследственный дефицит фактора VIII
D67– наследственный дефицит фактора IX
Гемофилия
 Версия: Клинические рекомендации РФ 2023 (Россия)
Версия: Клинические рекомендации РФ 2023 (Россия)
Общая информация
Краткое описание
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Возрастная категория: Взрослые, Дети
Пересмотр не позднее: 2025
Статус: Действует
Классификация
Таблица 1. Классификация гемофилии по степени тяжести

Около 60–70% всех диагностированных случаев гемофилии составляют тяжелые формы заболевания, для которых характерны спонтанные геморрагические эпизоды (преимущественно гемартрозы и гематомы мягких тканей различных локализаций). Степень тяжести нарушений свертывания крови и клинических проявлений при гемофилии зависит, как правило, от уровня активности фактора в крови, однако в клинической практике не всегда существует прямая корреляция между лабораторным и клиническим фенотипами заболевания.
Этиология и патогенез
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Основное проявление гемофилии – кровотечения и кровоизлияния, возникающие спонтанно или вследствие травмы (табл. 2). ГА и ГВ имеют схожую клиническую картину [1,3].
Таблица 2. Клинические проявления гемофилии

Гемофилия средней тяжести имеет сходные проявления. Первые признаки, как правило, развиваются после года. У пациентов с активностью факторов более 2% реже возникают кровоизлияния в суставы, забрюшинные гематомы, гематурии. Наиболее типичны посттравматические гематомы и длительные кровотечения, особенно при травмах слизистых оболочек.
Легкая гемофилия может никак не проявляться на протяжении всей жизни. Геморрагический синдром обычно возникает вследствие значительных травм или при хирургическом лечении. Поражение опорно-двигательного аппарата встречается чрезвычайно редко.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Для установления диагноза гемофилии у пациента с наличием геморрагического синдрома в анамнезе или при отягощенном семейном анамнезе используются критерии диагноза гемофилии (диагноз устанавливается при наличии как минимум двух из трех критериев) [1,3]:
Жалобы и анамнез
Лабораторные диагностические исследования
Получение максимального количества лабораторных данных способствует верификации диагноза и исключению приобретенных дефицитов факторов свертывания крови VIII/IX, а также исключению дефицитов других факторов свертывания крови.
Для экстренного контроля эффективности терапии необходимо использование теста АЧТВ (необходимо получить нормальные или субнормальные значения), однако эти данные не позволяют дифференцировать значения активности выше 30-50% и не отражают прямой корреляции с активностью факторов VIII и IX.
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
Классификация ингибиторов:
Ингибиторы в низком титре могут быть транзиторными и исчезать в течение 6 месяцев. Ингибиторы в высоком титре обычно носят постоянный характер. При длительном отсутствии заместительной терапии их титр может снизиться, но при возобновлении терапии может развиться анамнестическая реакция через 3–5 дней.
Инструментальные диагностические исследования
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Иные диагностические исследования
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
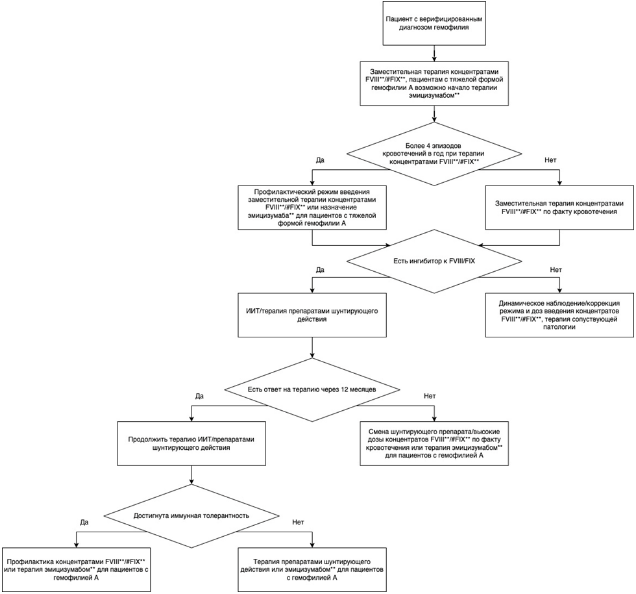
Общие принципы лечения
У ранее нелеченых пациентов целесообразно проводить терапию факторами свертывания крови, изготовленными из донорской плазмы или рекомбинантными концентратами факторов свертывания крови VIII/IX без смены терапии в течение 100 дней введений (при условии отсутствия выработки ингибитора). В настоящее время нет оснований для предпочтения той или иной группы факторов свертывания крови: плазматических (содержащих или не содержащих фактор Виллебранда) или рекомбинантных. При удовлетворительной эффективности и переносимости получаемой пациентом специфической терапии смена МНН факторов свертывания крови VIII или IX на протяжении жизни нецелесообразна.
Предпочтение должно отдаваться тому препарату, который при равной эффективности лучше всего переносится пациентом, имеет лучшие фармакокинетические индивидуальные показатели и наиболее удобен в использовании, исходя из конкретных объективных условий. Для индивидуального подбора препарата возможно у части пациентов проведение фармакокинетического исследования [20,21].
Использование неочищенных препаратов для профилактики или лечения кровотечений при гемофилии – компонентов крови (свежезамороженной плазмы или фактора свертывания крови VIII** в лекарственной форме раствора для инфузий [замороженного]) – возможно только в случаях, когда недоступен фактор свертывания крови, и не должно являться постоянной практикой [20,21].
Лечение кровотечений
Использование неадекватно низкой дозы и несоблюдение режима введения приводит к снижению эффективности, ухудшению состояния и увеличению расхода препарата. Неадекватно высокая доза может привести к развитию тромбозов и неоправданно повышает расход препарата.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
В некоторых случаях, например, при индивидуальных особенностях фармакокинетики в отсутствие ингибитора к FVIII или FIX), возможно применение более высоких доз факторов свертывания крови (B02BD по АТХ классификации) для купирования кровотечений.
Учитывая вариабельность фармакокинетических показателей у каждого конкретного пациента, заместительная терапия требует клинического и, при необходимости, лабораторного контроля. Клинический контроль должен проводиться врачом-гематологом при обращении пациента, родителями и самим пациентом постоянно. В основе клинического контроля лежит оценка динамики геморрагических проявлений и ее сопоставление с проводимой заместительной терапией. Лабораторный контроль проводится планово 1 раз в год и включает определение АЧТВ, активности дефицитного фактора в крови и наличие его ингибитора. Внеплановый лабораторный контроль проводится при обращении пациента по поводу снижения эффективности проводимой терапии и включает определение АЧТВ, активности дефицитного фактора в крови до и через 30 минут после введения расчетной дозы препарата (тест восстановления), наличие ингибитора. В ряде случаев дополнительно проводится фармакокинетическое исследование с определением активности FVIII/FIX по нескольким точкам с целью определения времени полужизни препарата. Для оценки результативности гемостатической терапии возможно у части пациентов проведение интегрального теста - тромбоэластографии [1,3].
Профилактическое лечение
Профилактическая терапия – необходимое условие сохранения физического и психологического здоровья пациентов с тяжелой и среднетяжелой гемофилией.
Первичная профилактика является наиболее эффективной для предотвращения поражения опорно-двигательного аппарата. Решение о начале постоянной профилактической заместительной терапии необходимо принимать с учетом состояния венозного доступа. При необходимости может решаться вопрос об установке центрального венозного катетера, который может быть имплантирован и использован только в случае возможности обеспечения адекватного обеспечения необходимыми расходными материалами, ухода и наблюдения пациента по месту жительства.
Вторичная профилактика начинается после двух или более гемартрозов при наличии минимальных признаков повреждения сустава. Третичная профилактика назначается в любом возрасте при наличии повреждения сустава/суставов. Может быть постоянной или краткосрочной (периодической).
Профилактическая терапия не устраняет уже развившееся повреждение сустава, но уменьшает частоту кровотечений и может замедлить прогрессирование артропатии и улучшить качество жизни.
Показаниями для проведения постоянной профилактической заместительной терапии факторами свертывания крови (B02BD по АТХ классификации) являются: тяжелая форма гемофилии, среднетяжелая форма гемофилии при развитии хотя бы одного эпизода гемартроза или выраженных геморрагических проявлений другой локализации. Пациентам с активностью фактора ≥5% постоянное или длительное профилактическое лечение необходимо при повторных кровоизлияниях в суставы, появлении признаков синовиита или артропатии, выраженных геморрагических проявлениях, требующих частых введений факторов свертывания крови.
Причинами недостаточно эффективной заместительной профилактической терапии могут быть: развитие ингибитора к фактору свертывания крови, назначение недостаточной дозы и/или кратности введения, несоблюдение режима введения и дозировок пациентом и родителями, индивидуальные особенности пациента, требующие применения более высоких доз или более частого введения препарата.
Решение о повышении дозы или кратности введения препарата при профилактической терапии должно быть принято, если имеются объективные клинические или лабораторные данные о ее неэффективности.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
При профилактическом лечении нонакогом альфа** у детей младше 12 лет, в зависимости от индивидуальных особенностей фармакокинетики, возраста, типа кровотечений, физической активности, в некоторых случаях могут использоваться более высокие дозы или укороченный интервал введения препарата [33]
Профилактическое введение любого препарата лучше проводить утром, чтобы максимальная активность фактора в крови была в период наибольшей активности. Протокол проведения профилактической терапии должен быть индивидуальным, насколько это возможно, в зависимости от возраста, венозного доступа, фенотипа кровотечений, активности фактора, коморбидности, социальной активности пациента и особенностей фармакокинетической кривой. В некоторых случаях (при повышенном травматизме, индивидуальных особенностях фармакокинетики в отсутствие ингибитора к FVIII) возможно применение более высоких доз факторов свертывания крови (B02BD по АТХ классификации) для профилактического лечения.
Особенности проведения гемостатической терапии в зависимости от локализации кровотечения
При развитии выраженного болевого синдрома возможно проведение кратковременной иммобилизации, которая должна сниматься сразу после прекращения болей.
При болевом синдроме показано использование местной гипотермии на 15 – 20 минут каждые 4 – 6 часов только в течение первых суток.
Реабилитационные мероприятия и ЛФК целесообразно начинать после прекращения болевого синдрома, учитывая локальный статус места повреждения.
Если пациент не получает постоянное профилактическое лечение, после купирования кровотечения показана кратковременная профилактика, особенно на время реабилитации.
Пункции сустава с аспирацией содержимого показаны при: гемартрозе с болевым синдромом, при наличии большого объема крови в полости сустава, при признаках развития гнойного артрита, развитии на фоне гемартроза нервно-мышечных нарушений.
У детей первых месяцев жизни возможны кровоизлияния с минимальными симптомами или бессимптомные. Даже минимальные кровоизлияния в ЦНС являются жизнеугрожающими, требуют экстренной госпитализации, интенсивной заместительной терапии и незамедлительного проведения КТ или МРТ головного мозга.
Следует регулярно контролировать показатели общего анализа крови и, при необходимости, проводить лечение анемии.
Для остановки кровотечения у пациентов с тяжелой формой ГА, получающих эмицизумаб**, рекомендовано применять дополнительно фактор свертывания крови VIII**/октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктоког альфа в стандартных дозировках в зависимости от локализации кровотечения. Для пациентов с гемофилией А, осложненной ингибиторами, получающих эмицизумаб**, препаратом первой линии для купирования кровотечения является эптаког альфа (активированный)** в стандартных дозах. Начальная доза антиингибиторного коагулянтного комплекса** не должна превышать 50 Ед/кг, и суточная доза не должна превышать 100 Ед/кг [45].
Лечение ингибиторной гемофилии
Появление ингибитора в основном проявляется отсутствием клинического ответа на стандартную терапию факторами свертывания крови (B02BD по АТХ классификации) или появлением кровотечений на профилактической терапии.
Поскольку при появлении ингибиторов стандартная заместительная терапия факторами свертывания крови VIII**/октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктокогом альфа, лоноктокогом альфа, руриоктокогом альфа пэгол или концентратом фактора свертывания крови IX**/нонакогом альфа**, албутрепенонакогом альфа становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше.
Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100–150 МЕ/кг препарата FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50–100 МЕ/кг препарата ежедневно или каждый второй день.
Снижение дозы и кратности введения препарата начинается после достижения следующих показателей: титр ингибитора - менее 0,6 БЕ, нормализация теста восстановления (более 66%) и нормализация периода полувыведения (более 7 часов). Снижение дозы препарата проводится постепенно по схеме с постоянным лабораторным контролем. После достижения дозы в 30–50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию в режиме вторичной/третичной профилактики в данной дозе длительно. Альтернативным вариантом профилактики после достижения толерантности является применение эмицизумаба** в стандартных режимах. Отмена профилактического лечения может привести к рецидиву ингибитора. Максимальная длительность ИИТ 3 года. Критерии эффективности ИИТ представлены в таблице 3.
Таблица 3. Критерии эффективности ИИТ

При проведении ИИТ необходимо избегать любых воздействий и препаратов, стимулирующих иммунные реакции, в том числе вакцинации, применения препаратов интерферона и других видов иммунотерапии.
Опыт проведения ИИТ у пациентов с ингибиторной ГB ограничен. Это обусловлено очень низкой эффективностью и аллергическими реакциями.
Лечение ортопедических осложнений гемофилии
Хроническая деформирующая артропатия возникает вследствие прогрессирующего течения хронического синовиита и рецидивирующих кровоизлияний в суставы. Проявляется остеопорозом, нарушением структуры, истончением и потерей суставного хряща, болевым синдромом, контрактурами, мышечной атрофией, деформацией сустава.
Основой профилактики развития хронической артропатии является адекватная постоянная профилактическая заместительная терапия. Своевременное лечение синовиита также необходимо для предотвращения развития артропатии. Диагностика артропатии основана на выявлении клинических признаков и на результатах проведенных инструментальных исследований: УЗИ, КТ, МРТ.
Целью лечения уже развившейся хронической артропатии является улучшение функционирования сустава и уменьшение болевого синдрома. Для борьбы с болевым синдромом у пациентов старше 18 лет оптимально использовать оксикамы (ингибиторы ЦОГ-2, M01AC по АТХ классификации) (отдельные препараты из группы НПВП (M01A нестероидные противовоспалительные и противоревматические препараты), а именно кеторолак**, нимесулид, ибупрофен**, препараты из группы «коксибы» (М01АН по АТХ классификации).У детей с массой тела более 5 кг возможно применение препарата ибупрофен**, у детей в возрасте старше 2 лет возможно применение препарата нимесулид, у детей в возрасте старше 16 лет возможно применение препарата кеторолак**.[46]. Для восстановления функции сустава и состояния мышц проводят курсы ЛФК и физиотерапии. В ряде случаев эффективно использование тренажеров. На начальных этапах восстановительного лечения показано проведение курсов гиалуроновой кислоты в комбинации с препаратами из группы S01KA51 гиалоурановая кислота в комбинации с другими средствами по АТХ классификации. При недостаточной эффективности консервативной терапии, показано хирургическое лечение. Хирургическое лечение пациентов с гемофилией должно проводиться врачами, имеющими опыт лечения пациентов с гемофилией.
Диагностика включает выявление клинических признаков, УЗИ суставов и/или МРТ. Терапия проводится совместно с врачами-травматологами-ортопедами, имеющими опыт лечения больных гемофилией. При сохранении признаков воспаления, пациентам старше 18 лет, показана терапия оксикамами (ингибиторами ЦОГ-2) (отдельными препаратами из группы НПВП, а именно кеторолак**, нимесулид, ибупрофен**, препараты из группы «коксибы» (М01АН по АТХ классификации У детей с массой тела более 5 кг возможно применение препарата ибупрофен**, у детей в возрасте старше 2 лет возможно применение препарата нимесулид, у детей в возрасте старше 16 лет возможно применение препарата кеторолак**.[46].
При недостаточной эффективности заместительной терапии возможно проведение курса пункций сустава с введением стероидных противовоспалительных препаратов (на первом этапе), далее, вариантами выбора являются химическая или эндоскопическая синовэктомия, а при их недостаточной эффективности – хирургическая коррекция.
Ведение пациентов с гемофилией и псевдоопухолями должно осуществляться совместно врачами-хирургами и врачами-гематологами.
При отсутствии лечения псевдоопухоль может достигать гигантских размеров, создавая давление на нейроваскулярные структуры и вызывая патологические переломы.
Операция должна проводиться специалистами, имеющими опыт хирургического ортопедического лечения больных гемофилией.
Оперативное лечение
При необходимости проведения таких диагностических процедур, как спинномозговая пункция, пункция артерии, эндоскопическое исследование с биопсией, ведение пациента такое же, как при хирургическом лечении.
Пациентам, получающим профилактическое лечение эмицизумабом**, рекомендовано проводить любое оперативное вмешательство или инвазивную процедуру без отмены препарата с применением стандартных доз фактора свертывания крови VIII**/фактора свертывания крови VIII + фактор Виллебранда**/ октокога альфа**/мороктокога альфа**/симоктокога альфа (фактор свертывания крови VIII человеческий рекомбинантный)**[49]/лоноктокога альфа/туроктокога альфа/эфмороктокога альфа**/руриоктокога альфа пэгол. Для пациентов с ГА, осложненной ингибиторами и получающих эмицизумаб**, препаратом выбора является эптаког альфа (активированный)** в стандартных дозах. При необходимости назначения антиингибиторного коагулянтного комплекса** начальная доза не должна превышать 50 Ед/кг, и суточная доза не должна превышать 100 Ед/кг [50].
Длительный сосудистый доступ у пациентов с гемофилией
Показания к использованию устройства долговременного центрального венозного доступа является:
Абсолютным противопоказанием к установке устройства долговременного центрального венозного доступа является наличие у пациента признаков активной инфекции.

Основные принципы организации помощи пациентам с гемофилией
Гарантированное бесперебойное обеспечение факторами свертывания крови VIII** и FIX**, фактором свертывания крови VIII + фактор Виллебранда**, октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VII человеческий рекомбинантный)**, нонакогом альфа**, лоноктокогом альфа, туроктокогом альфа, эфмороктокогом альфа**, руриоктокогом альфа пэгол, албутрепенонакогом альфа, эмицизумабом** у пациентов с неосложненной гемофилией или препаратами шунтирующего действия, эмицизумабом** у пациентов с ингибиторной формой гемофилии A, обучение применению этих препаратов членов семьи больных гемофилией является приоритетом в организации помощи больным гемофилией.
Стоматологическая помощь
При оказании стоматологической помощи важно тесное взаимодействие врача- стоматолога и врача-гематолога. Удаление зуба или хирургические процедуры выполнять под строгим контролем гемостаза и после консультации врача-гематолога.
При проведении стоматологических процедур возможно применение транексамовой кислоты** (за исключением детей младше 1 года) или других антифибринолитические средства с целью уменьшения необходимости в заместительной терапии факторами свертывания крови. Возможно использование гемостатических средства для местного применения после удаления зубов. При обширных стоматологических процедурах (наложение швов, множественная экстракция зубов) может понадобиться госпитализация пациента в стационар.
Следует воздержаться от применения НПВП, особенно ацетилсалициловой кислоты**.
Особого внимания требует профилактика во время стоматологических процедур у пациентов с ингибиторами к фактору VIII/IX.
Гемофилия у новорожденных.
Проведение лабораторных исследований
Вакцинация.
Пациенты с гемофилией могут быть вакцинированы. Особенно важно проведение вакцинации от гепатита В. При вакцинации предпочтение отдается оральному или подкожному введению препарата, по сравнению с внутримышечным или внутрикожным. Если для данной вакцины доступен только внутримышечный путь введения, необходима заместительная терапия для предотвращения развития гематомы. В этом случае заместительную терапию проводят накануне вакцинации. В день вакцинации введение препарата не рекомендуется. Нельзя проводить вакцинацию во время кровотечения.
Нежелательная медикаментозная терапия.
Применение таких препаратов может привести к развитию тяжелых кровотечений, которые не контролируются введением факторов свертывания крови. Однако, развившийся тромбоз может потребовать применения антитромботических средств (антикоагулянтов, B01A по АТХ классификации). Предпочтение надо отдавать препаратам кратковременного действия. Каждый раз необходимо анализировать соотношение пользы и риска от применения антитромботических средств (антикоагулянтов и ингибиторов агрегации тромбоцитов).
Обучение пациентов и членов их семей.
Обучение пациентов и членов их семей – необходимое условие обеспечения адекватной помощи таким больным. Обучение начинается сразу после установления диагноза и проводится на постоянной основе врачами и медицинскими сестрами центра, в котором наблюдается пациент.
Обучение проводится индивидуально при посещении центра и в рамках школы больных гемофилией.
Основные направления обучения пациента и членов его семьи:
Помимо врачей и медсестер к обучению пациентов и членов их семей необходимо привлекать медицинских психологов, юристов и членов общественных организаций, представляющих интересы больных гемофилией.
Медицинская реабилитация
Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
Возможны такие виды терапии как:
Госпитализация
Организация оказания медицинской помощи
Всех пациентов с гемофилией рекомендовано регистрировать и наблюдать в специализированном центре (по возможности). Должна быть круглосуточная возможность контакта с врачом-гематологом, имеющим опыт лечения больных с нарушениями гемостаза.
Показания для плановой госпитализации:
Показания для экстренной госпитализации:
Показания к выписке пациента из стационара:
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Пациенты с гемофилией должны наблюдаться группой специалистов различного профиля, включающей врача-гематолога, врача-педиатра, врача-травматолога-ортопеда, врача-стоматолога, врача-физиотерапевта, врача ЛФК, медицинского психолога, имеющих опыт работы с больными гемофилией [1,24].
Лечение осложнений гемофилии: коррекция дефицита железа, ингибиторов.
Выявление сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов, патологии сердечно-сосудистой системы и др. и направление к профильным специалистам.
Информация
Источники и литература
Информация
Список сокращений

Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Конфликт интересов: отсутствует
Приложение А2. Методология разработки клинических рекомендаций
Методы, использованные для сбора/селекции доказательств:
Базы данных, использованных для сбора/селекции доказательств:
Методы, использованные для анализа доказательств:
Методы, использованные для качества и силы доказательств:
Методология разработки рекомендаций:
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология должна быть изучена для того, чтобы убедиться в соответствии ее принципам доказательной медицины. Результат изучения влияет на уровень доказательности, присваиваемый публикации, что в свою очередь влияет на силу вытекающих из нее рекомендаций.
Методологическое изучение фокусируется на особенностях дизайна исследования, которые оказывали существенное влияние на качество результатов и выводов.
Методы, использованные для формулирования рекомендаций:
Методология валидизации рекомендаций:
Описание методики валидизации рекомендаций:
Рекомендации в предварительной версии рецензируются независимыми экспертами, которых просят прокомментировать, насколько качественно интерпретированы доказательства и разработаны рекомендации. Также проводится экспертная оценка стиля изложения рекомендаций и их доступности для понимания.
Предварительные версии рекомендаций представляются для обсуждения на научных гематологических конференциях Национального гематологического общества и заседаниях Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, ведущими специалистами профильных Федеральных центров РФ и практическими врачами.
Изучаются комментарии со стороны врачей-гематологов амбулаторного и стационарного этапов в отношении доходчивости и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Замечания и комментарии, полученные от экспертов, тщательно систематизируются и обсуждаются авторским коллективом. При необходимости проводится внесение изменений и дополнений в текст рекомендаций.
Окончательная редакция:
Окончательная редакция клинических рекомендаций рассматриваются и утверждаются на заседании Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, и в заключении, на конгрессе (съезде, пленуме) национального гематологического общества.
Таблица А2.1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
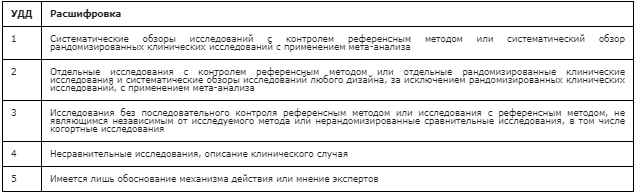
Таблица А2.2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)

Таблица А2.3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)

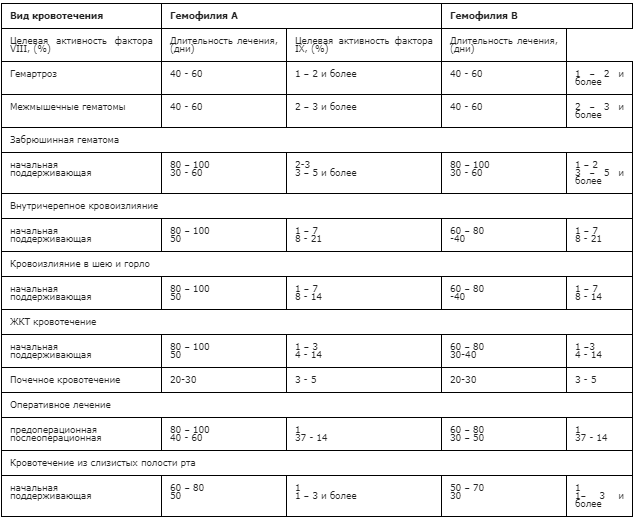
Приложение А3.1. Рекомендуемая активность фактора и продолжительность терапии при различных видах кровотечений




Приложение В.4 Паспорт пациента с гемофилией
ПАСПОРТ БОЛЬНОГО ГЕМОФИЛИЕЙ
Владелец данного документа страдает пониженной свертываемостью крови, получает внутривенные инъекции антигемофильными препаратами. При нём могут быть лекарственные препараты и средства для их внутривенного введения.

Прикреплённые файлы
Внимание!
