Гепатобластома у детей
Гепатобластома у детей
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Общая информация
Краткое описание
Одобрено Научно-практическим Советом Минздрава РФ
– размещенные в Рубрикаторе после 1 января 2024 года – с 1 января 2025 года.
Клинические рекомендации
Возрастная категория: Дети
Пересмотр не позднее: 2026
ID: 68
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Гепатобластома группы стандартного риска - локализованные опухоли (PRETEXT I, II и III) без дополнительных неблагоприятных критериев, таких как:
Гепатобластома группы высокого риска – локализованные опухоли, не подпадающие под критерии группы стандартного риска и группы очень высокого риска. Как правило, в данную группу попадают пациенты с распространенным поражением печени - PRETEXT II, PRETEXT III, PRETEXT IV с вовлечением магистральных сосудов.
Метастазы легких – доказанными метастазами являются следующие изменения по данным РГ и КТ органов грудной клетки: один очаг без кальцификатов размером 5 мм и более, два и более очага без кальцификатов размером более 3 мм [14].
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза: диагноз ГБ может быть установлен на основании анализа данных:
При проведении визуализационных методов исследования целесообразно использование контрастного усиления для детального выявления очаговых изменений в исследуемых анатомических областях, а также оценка особенностей контрастирования очаговых изменений в различные фазы контрастирования (артериальная, венозная, отсроченные фазы) [13].
1. Жалобы и анамнез
2. Физикальное обследование
3. Лабораторные диагностические исследования
1. Лабораторные исследования для оценки общего состояния пациента
2. Лабораторные исследования для верификации диагноза и оценки прогностических факторов
4. Инструментальные диагностические исследования
Интерпретация КТ-снимков грудной клетки может быть затруднена из-за ателектазов легких (обычно в базальных отделах), которые могут возникать из-за седации и анестезии, и/или из-за компрессии большой опухолью в печени. В сомнительных случаях обсудите с анестезиологом возможность повторного исследования в положении пациента лежа на животе. Если по-прежнему остаются сомнения относительно метастатического поражения легких, целесообразно провести референс визуализации в специализированном центре/клинике.
Другие визуализирующие исследования: ангиография сосудов органов брюшной полости, сцинтиграфия печени и селезенки, позитронно-эмиссионная томография (ПЭТ-КТ), и внутривенная урография не используются в качестве стандартных процедур при обследовании детей с предполагаемой опухолью печени, однако могут быть использованы для уточнения распространенности опухоли и принятия решения об объеме терапии.
При планировании и проведении инициальных и контрольных визуализационных методов исследования необходимо учитывать следующие особенности:
5. Иные диагностические исследования
У пациентов в возрасте от 6 месяцев до 3 лет (2 года 11 месяцев 30 дней) проведение биопсии опухоли может не проводиться в ситуации, когда тяжесть состояния пациента не позволяет провести хирургическое вмешательство, при условии ясной клинической картины, включающей солидную опухоль печени, подтвержденную данными анатомической визуализации и динамическом повышением уровня АФП в сыворотке крови (измерение проводится не менее двух раз и уровень АФП должен превышать в три и более раза верхние пороговые значения для данной возрастной группы).
Допустимо первичное удаление опухоли в объеме анатомической резекции печени при соблюдении условии гарантированного радикального удаления опухоли. Первичное удаление опухоли может рассматриваться у пациентов с солитарными (один очаг) опухолями, имеющими преимущественно “краевое” расположение с малым интрапаренхиматозным компонентом, или опухолями, расположенными преимущественно интрапаренхиматозно, при условии, что их радиологические характеристики соответствуют признакам гепатобластомы, распространение затрагивает не более двух сегментов или одного сектора печени и отсутствуют признаки сосудистой инвазии. (стратификация пациента в группу стандартного риска).
Решение о проведении первичной резекции должно приниматься в рамках мультидисциплинарного консилиума с участием детских хирургов, детских онкологов и специалистов по визуализации ТОЛЬКО в федеральных центрах, специализирующихся на лечении пациентов с опухолями печени и использующими настоящие клинические рекомендации.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Для определения группы риска и принятия решения о назначении риск – адаптированной программы противоопухолевого лечения целесообразно проведение консилиума в составе: врача - детского онколога, врача-рентгенолога и врача-детского хирурга. При необходимости в мультидисциплинарный консилиум привлекаются дополнительные специалисты. В случаи распространенности PRETEXT III-IV – обязательная консультация пациента в трансплантационном центе не позднее одного месяца от начала терапии.
1. Лечение детей с гепатобластомой группы стандартного риска (см. Приложение Б).
План лечения включает следующие фазы:
Пациентам с ГБ группы стандартного риска рекомендовано в рамках лечения по протоколу SIOPEL-3 SR (стандартный риск) на первом этапе проведение предоперационной терапии препаратом #цисплатин** 80 мг/м2 в объеме 4 курсов с 14 дневным интервалом [12, 68] на фоне инфузионной терапии 3 л/м2 в течение 24 часов растворами 5% #декстрозы** и 0,9% раствора натрия хлорида**. Обязательным является добавление в инфузионные растворы электролитов:
Всем пациентам со стадией распространенности опухолевого процесса PRETEXT III-IV и/или с вовлечением магистральных сосудов, соответствующим V3 или P2, поражением первого сегмента печени (хвостатой доли, критерий С) необходима обязательная консультация пациента в трансплантационном центре не позднее одного месяца от начала терапии.
На разных фазах терапии проводится оценка изменений размеров опухоли ответа опухоли с оценкой резектабельности и/или статуса ремиссии согласно рекомендациям, описанным ниже.
Также можно рекомендовать режим введения #цисплатина** в виде внутривенной инфузии за 6 часов. Можно рекомендовать режим введения #доксорубицина** в виде внутривенной инфузии за 6 часов на день 15-16, 43-44 и 71-72 (в/в, 6-часовая непрерывная инфузия, то есть по 30 мг/м2/сутки в течение двух дней) [68] на фоне инфузионной терапии 3 л/м2 в течение 24 часов растворами 5% #декстрозы** и 0,9% раствора натрия хлорида**.
Обязательным является добавление в инфузионные растворы электролитов:
Если операция невозможна после дня 85 предоперационной фазы полихимиотерапии, но опухоль продолжает отвечать на химиотерапию, пациенту проводится еще, максимум, два введения #карбоплатина**/#доксорубицина**, чередующихся с одним введением #цисплатина**. Возможность радикальной операции будет оценена в конце данных дополнительных курсов химиотерапии.
Также возможен режим введения #цисплатина** и #доксорубицина** в виде внутривенной инфузии за 6 часов. В случае введения #доксорубицина** в виде внутривенной инфузии за 6 часов, препарат вводится в дозе 30 мг/м2/сутки в течение двух дней [68] на фоне инфузионной терапии 3 л/м2 в течение 24 часов растворами 5% #декстрозы** и 0,9% раствора натрия хлорида**. Обязательным является добавление в инфузионные растворы электролитов:
Завершение терапии целесообразно после проведения суммарно 10 курсов химиотерапии (5 курсов по схеме #карбоплатин**/#доксорубицин** и 5 доз #цисплатина**) в сочетании с радикальным удаление опухоли.
3. Лечение детей с гепатобластомой группы очень высокого риска (см. Приложение Б)
Метастазы легких – доказанными метастазами являются следующие изменения по данным РГ и КТ органов грудной клетки: один очаг без кальцификатов размером 5 мм и более, два и более очага без кальцификатов размером более 3 мм. Во всех остальных случаях очаги рассматриваются как сомнительные. В этих ситуациях целесообразно рассмотреть вопрос о биопсии очаговых образований легкого [14].
На разных фазах проводится оценка ответа опухоли, резектабельности и/или статуса ремиссии согласно рекомендациям, описанным ниже.
Предоперационная (неоадъювантная) химиотерапия – БЛОК А1 [67]:
При массе тела ребенка менее 10 кг необходимо рассчитывать дозы препаратов на массу тела.
В случае начала курса ПХТ, его необходимо довести до конца вне зависимости от результатов анализов крови во время курса. Единственной причиной остановки лечения является наличие токсичности 4 степени или угрожающих жизни осложнений.
При массе тела ребенка менее 10 кг необходимо рассчитывать дозы препаратов на массу тела.
При массе тела ребенка менее 10 кг необходимо рассчитывать дозы препаратов на массу тела.
2. Хирургическая тактика лечения пациентов с метастазами в легкие.
Послеоперационную химиотерапию следует начать, как только пациент восстановится после операции. Пациентам, которым выполнена трансплантация печени после БЛОКОВ A1 – A3, также показана послеоперационная химиотерапия, только если нет ярко выраженных хирургических или иммунологических противопоказаний.
4. Лечение микроскопической остаточной болезни
5. Проведение сопутствующей и сопроводительной терапии
6. Нутрициологическое сопровождение.
Таблица 1. Интерпретация нутритивного статуса на основании Z-score согласно референсным данным ВОЗ [79, 83]
Показатели *
Ожирение морбидное
+4,00 и выше
Примечания: нутритивный статус в онкопедиатрии оценивается по совокупным данным (клинические, лабораторные, инструментальные), с учетом нутритивного риска, антропометрические показатели позволяют критериально ориентироваться в определении нутритивного статуса и не могут быть единственно определяющими [83]; *– в определении нутритивного статуса используется показатель с минимальным SDS; SDS – standard deviation score (величина стандартного отклонения), ожирение – простое; гипоталамическое; при нейроэндокринных заболеваниях; ятрогенное; моногенное; синдромальное
Таблица 2. Факторы высокого риска развития нарушений нутритивного статуса [83]
Критерии
При наличии минимум двух вышеперечисленных критериев пациент относится к группе высокого нутритивного риска – вне зависимости от текущего нутритивного статуса, его текущего питания и клинической ситуации
Таблица 3. Основные скрининговые инструменты для выявления риска нутритивных нарушений в педиатрии [83, 94]
Скрининговый инструмент
Данные, необходимые для оценки риска
Определение степени острой и хронической БЭН
Антропометрические данные
Простая педиатрическая шкала для выявления детей с риском недоедания (PNRS)
Инструмент скрининга для оценки недоедания в педиатрии (STAMP)
Инструмент скрининга нутритивного риска у детей в стационаре (STRONGkids)
Детская шкала недоедания по Йоркиллу (PYMS)
Инструмент нутритивного скрининга для детской онкологии (SCAN)
Субъективная глобальная оценка питания (SGNA)
Таблица 4. Рекомендуемые потребности детей в основных нутриентах и энергии (на кг массы тела в сутки) при расчете диетотерапии и энтерального питания [95]
Возраст
Новорожденные
1,5 – 4
3 - 4
18
110 - 120
до 1 года
1 - 2,5
3 - 4
16 – 18
90 - 100
1-2 года
12 – 14
75 - 90
3-6 лет
10 – 12
75 - 90
7-12 лет
до 12
60 - 75
13-18 лет
до 10
30 - 60
Примечания: Потребности приведены для ориентировки расчета и назначения энтерального питания; они не отменяют и не заменяют пациент-ориентированный подход в назначении нутритивной поддержки: в каждом конкретном случае следует учитывать клиническую картину, возможные метаболические и органные дисфункции и корректировать поступление нутриентов с учетом возможности и переносимости ребенком
7. Гемотрансфузионная поддержка
8. Венозный доступ.
Рекомендации по выбору устройства
Не существует достаточных доказательств для однозначного преимущества одного устройства перед другим для каждой категории пациентов. Желательно использовать катетер с наименьшим числом просветом [108].
Для постоянного использования (ежедневно или хотя бы один раз в неделю) рекомендуется применять внешние катетеры такие как PICC, CICC и FICC, для периодического использования (реже одного раза в неделю) – полностью имплантированные системы (порт) [109].
Рекомендации по установке устройства
Подробное описание имеется в клинических рекомендациях ФАР [111].
Введение катетера путем хирургического разреза вены не желательно у пациентов, страдающих онкогематологическими заболеваниями [114]
Для катетеров из полиуретана используется цианакрилатный тканевой клей [115], для силиконовых катетеров он в практике не используется [116]
Уход за венозным доступом и его удаление.
9. Профилактика и лечение тошноты и рвоты, обусловленных проведением противоопухолевой терапии.
1. Определение уровня эметогенности и варианта профилактики ТИР
2. Профилактика тошноты и рвоты на фоне высокоэметогенной химиотерапии
Если в режим противоопухолевой терапии входит глюкокортикоид в дозе равной или превышающей дозу, показанную к использованию с противорвотной целью, дополнительного (к режиму противоопухолевой терапии) введения глюкокортикоида для профилактики ТИР в этот день не требуется.
5. Лечение прорывной и рефрактерной рвоты
Если прорывная ТИР возникла на фоне цитостатической терапии (и соответственно профилактики), относящейся к минимально, низко- или среднеэметогенному уровню, то необходимо использовать препараты, предусмотренные следующим, более высоким уровнем профилактики.
Если пациент и так получает профилактику, предусмотренную для высокоэметогенной терапии, то при возникновении прорывной ТИР необходимо рассмотреть вопрос о добавлении #оланзапина** (если он не применялся ранее в связи с неподходящим возрастом или массой тела). При невозможности использовать #оланзапин** в качестве альтернативы может быть применен метоклопрамид.
6.
Таблица 1 - Уровень эметогенности противоопухолевых препаратов
Степень эметогенности (риск развития рвоты)
Высокая (>90%)
Монотерапия
Комбинированные режимы
Монотерапия
Комбинированные режимы
Монотерапия
Комбинированная терапия
Цитарабин** (в/в) 60 мг/м2 + метотрексат** (в/в) 90 мг/м2
Минимальная (<10%)
Монотерапия
Комбинированные режимы
Меркаптопурин** (р.о.) ≤ 2.5 мг/кг +метотрексат** (р.о.) ≤ 0.1 мг/кг/сутки
Цисплатин** ≤ 60 мг/м2 (в/а) + доксорубицин** ≤ 30 мг/м2 (в/а)
7.
Таблица 2 - Дозы и режимы противорвотных препаратов
Степень эметогенности
Режимы
Дозы
Высокая
Умеренная
Блокаторы серотониновых 5HT3-рецепторов (палоносетрон)
Низкая
Блокаторы серотониновых 5HT3-рецепторов
Минимальная
10. Профиллактика и диагностика инфекции у детей с гепатобластомой на фоне проводимого лечения.
Используемые стандартные определения
2. Иные диагностические исследования
3. Лечение при фебрильной нейтропении
- Целесообразные варианты эмпирической антибиотикотерапии:
- В клиниках с низкой частотой детекции энтеробактерий с продукцией БЛРС допустимо назначение:
- Назначение ванкомицина** в дополнение к базовому препарату в первой линии терапии показано при развитии язвенно-некротического стоматита, поражении мягких тканей, подозрении на катетерную инфекцию (до получения микробиологического подтверждения), у пациентов после проведения ХТ с применением высоких доз цитарабина, а также в случае предшествующей колонизации пациента метициллин-резистентным золотистым стафилококком (МРЗС);
-При подозрении на развитие анаэробной инфекции (гингивит, целлюлит периоральной области, интраабдоминальная или параректальная инфекция) необходимо назначение антибиотиков, обладающих антианаэробной активностью (пиперациллин/тазобактам, имипенем/циластатин**, метронидазол**, клиндамицин**).
- При аллергии на бета-лактамные антибиотики в качестве альтернативной схемы могут быть назначены фторхинолоны либо азтреонам** в сочетании с ванкомицином** или клиндамицином**:
При развитии признаков сепсиса и септического шока следует назначить антибиотики наиболее широкого спектра действия: карбапенемы в сочетании с аминогликозидами и ванкомицином**, а пациентам с известной колонизацией – препараты группы резерва. При развитии тяжелых инфекционных осложнений и/или сепсиса антибактериальные препараты назначаются в максимальных дозах, предпочтительно пролонгированными инфузиями в связи с нарушением клиренса и перераспределением жидкости в организме [166 – 168].
Эмпирическое назначение противогрибковых препаратов
Терапия выбора при развитии инвазивного аспергиллеза:
Терапия выбора при развитии инвазивного мукормикоза:
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Госпитализация
Организация оказания медицинской помощи
Показания к выписке пациента из медицинской организации
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Таблица 5.1.
Комплексный клинико-лабораторный и инструментальный мониторинг у пациентов с гепатобластомой группы стандартного риска, окончивших специфическую терапию (модифицированная версия в рамках протокола SIOPEL3 SR).
Срок от окончания лечения
Исследование
1 год
2 год
3 год
год
Более 5 лет
Диспансерный прием (осмотр, консультация) врача-педиатра и врача-детского онколога
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Общий (клинический) анализ крови развернутый, Общий (клинический) анализ мочи
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Определение уровня АФП в сыворотке крови
1 раз в месяц в первые 6 мес, далее 1 раз 2 мес (суммарно 9 раз)
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Анализ крови биохимический общетерапевтический
1 раз в 2 мес.
1 раза в 2 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в год
1 раз в 3 мес.
1 раза в 6 мес.
1 раз в 6 мес.
1 раз в год
1 раз в год
УЗИ органов брюшной полости (комплексное)
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Компьютерная томография/Магнитно-резонансная томография органов брюшной полости с внутривенным болюсным контрастированием
При повышении уровня АФП, изменениях при проведении УЗИ, подозрительных на развитие рецидива
Тональная аудиометрия
1 раз в год
1 раз в год
1 раз в год
1 раз в год
1 раз в год
Таблица 5.2.
Комплексный клинико-лабораторный и инструментальный мониторинг у пациентов с гепатобластомой группы высокого риска и группы очень высокого риска, окончивших специфическую терапию (модифицированная версия в рамках протоколов SIOPEL-3 HR и SIOPEL4).
Исследование
Срок от окончания лечения
2 год
3 год
4 год
Более 5 лет
Диспансерный прием (осмотр, консультация) врача-педиатра и врача-детского онколога
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Общий (клинический) анализ крови развернутый, Общий (клинический) анализ мочи
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Определение уровня АФП в сыворотке крови
1 раз в месяц (суммарно 12 раз)
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Анализ крови биохимический общетерапевтический
1 раз в 2 мес.
1 раз в 2 мес..
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Исследование функции нефронов по клиренсу креатинина (проба Реберга)
1 раз в год
При уровне <80 мл/мин/1,72 кв.м. площади поверхности тела ежегодно
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
1 раз в год
УЗИ органов брюшной полости
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Компьютерная томография/Магнитно-резонансная томография органов брюшной полости с внутривенным болюсным контрастированием
Тональная аудиометрия
1 раз в год
1 раз в год
1 раз в год
1 раз в год
1 раз в год
ЭХО-КГ
1 раз в 6 мес.
1 раз в год
1 раз в год
1 раз в год
1 раз в год
Таблица 5.3.
Комплексный клинико-лабораторный и инструментальный мониторинг у пациентов с гепатобластомой после трансплантации печени (неосложненном течении), окончивших специфическую терапию.
Исследование
Срок от окончания лечения
2 год
3 год
4 год
Более 5 лет
Диспансерный прием (осмотр, консультация) врача-педиатра и врача-детского онколога
1 раз в 1 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в год
Мониторинг АД
ежедневно
ежедневно
ежедневно
ежедневно
ежедневно
Общий (клинический) анализ крови развернутый, Общий (клинический) анализ мочи
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
Анализ крови биохимический общетерапевтический 1
1 раз в 2 мес.
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
Коагулограмма
1 раз в 4 мес.
1 раз в 4 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
Определение уровня АФП в сыворотке крови
1 раз в месяц (суммарно 12 раз)
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 6 мес
1 раз в 6 мес.
Концентрация ИК (такролимус** или циклоспорин А**)
1 раз в месяц
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
Определение антител к цитомегаловирусу (Cytomegalovirus) в крови, Определение антител классов M, G (IgM, IgG) к вирусу Эпштейна-Барра (Epstein - Barr virus) в крови, Определение антител к вирусу простого герпеса (Herpes simplex virus) в крови, Определение антител класса G (IgG) к вирусу простого герпеса 1 типа (Herpes simplex virus 1) в крови, Определение антител класса G (IgG) к вирусу простого герпеса 2 типа (Herpes simplex virus 2) в крови, Определение антител класса M (IgM) к вирусу простого герпеса 1 и 2 типов (Herpes simplex virus types 1, 2) в крови, Определение антител к вирусу герпеса человека 6 типа (Herpesvirus 6) в крови
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в год
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
1 раз в год
ЭКГ, ЭХО-КГ
1 раз в 6 мес.
1 раз в год
1 раз в год
1 раз в год
1 раз в год
Ультразвуковое исследование органов брюшной полости (комплексное) с дуплексным сканированием сосудов печени
1 раз в 2 мес.
1 раз в 3 мес.
1 раз в 3 мес.
1 раз в 6 мес.
1 раз в год
Магнитно-резонансная томография органов брюшной полости с внутривенным болюсным контрастированием
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в год.
По показаниям
По показаниям
Тональная аудиометрия
1 раз в год
1 раз в год
1 раз в год
1 раз в год
1 раз в год
Электроэнцефалограмма, прием (осмотр, консультация) врача-невролога
1 раз в год
1 раз в год
1 раз в год
1 раз в год
1 раз в год
Прием (осмотр, консультация) врача-стоматолога детского, санация ротовой полости
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
Не реже 1 раза в год
Прием (осмотр, консультация) врача-офтальмолога (глазные среды, глазное дно)
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
1 раз в 6 мес.
Не реже 1 раза в год
ирубин, общий белок, глюкоза, альбумин, мочевина, креатинин, АСТ, АЛТ, ЩФ, исследование активности гамма-глютамилтрансферазы в крови, амилаза, исследование липидограммы, мочевая кислота, электролиты сыворотки крови (калий, натрий, кальций, магний), гликозилированный гемоглобин, исследование уровня сывороточного железа сыворотки крови, исследование насыщение насыщения трансферина железом, исследование железосвязывающей способности сыворотки
Информация
Источники и литература
Информация
Термины и определения
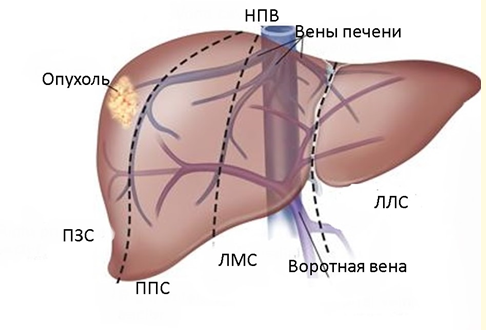
Анатомическая граница между ЛЛС (LLS) и ЛМС (LMS) - круглая связка печени и вертикальная ветвь ЛВВ, между ЛМС и ППС - срединная вена печени и ложе желчного пузыря. ППС и ПЗС отграничены правой печеночной веной.
Описание стадий по системе PRETEXT
PRETEXT II - два смежных сектора не поражены. Мультифокальные опухоли с поражением ЛЛС (LLS) и ПЗС (RPS), изолированные опухоли ЛМС (LMS) или ППС (RAS) так же относятся к PRETEXT II.

Опухоли правой доли печени, как правило, имеют большие размеры. Большое значение имеет динамический контроль после курсов ПХТ, тогда правильному стадированию опухоли помогает дифференциация и топография срединной вены (СВ).
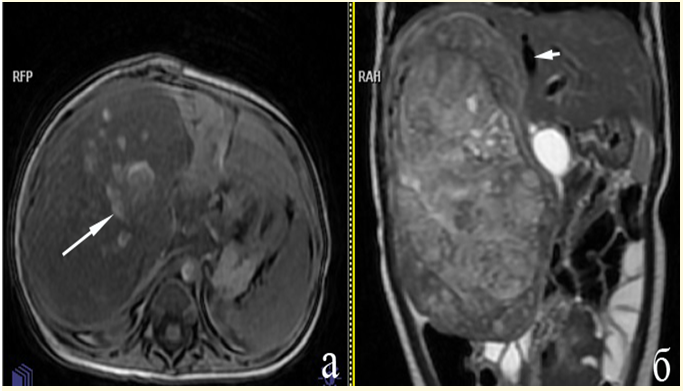
Рисунок 7.1.4. Пациент, 11 мес. ГБ правой доли печени, PRETEXT II. (а) – на Т1-ВИ: образование правой доли печени, с участками кровоизлияний (стрелка); (б) – Т2-ВИ: ГБ гетерогенной структуры, по медиальному краю образования дифференцируется СВ печени (короткая стрелка).
PRETEXT III - нет непораженных двух смежных секторов печени. Монофокальные (одноузловые) опухоли в этой категории обычно достигают большого объема (рис. 6), оставляют свободными только ЛЛС (LLS) и/или ПЗС (RPS).
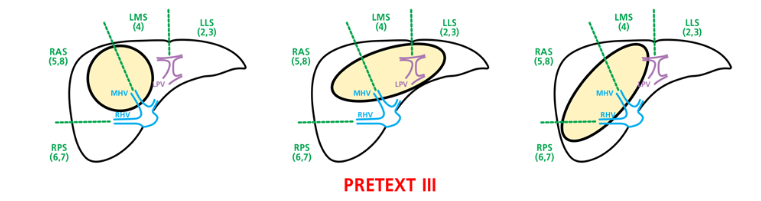
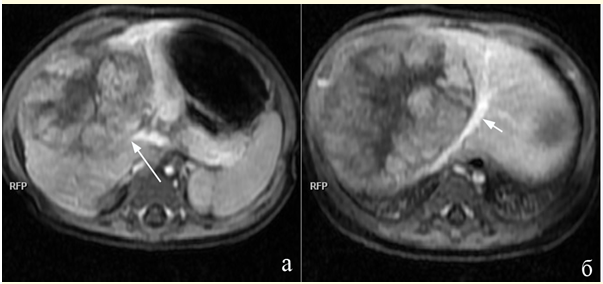
Основная задача исследования с контрастным усилением – отличить инвазию сосуда от его компрессии и минимальную вовлеченность в опухолевый процесс прилежащих участков паренхимы печени, поскольку от этого зависит стратификация риска. Отсутствие визуализации и контрастирования воротной вены или ее ветвей является убедительным доказательством ее инвазии. Составляющими высокого риска является поражение двух ветвей воротной вены или ствола воротной вены, а также инвазия одной ветви ВВ в сочетании с поражением собственных вен печени (рис. 7.1.7).
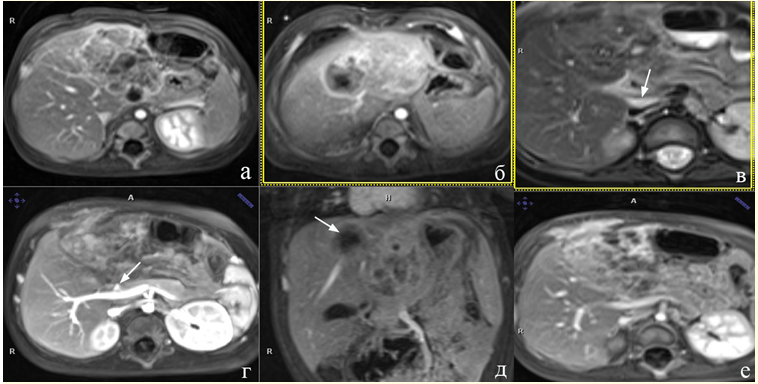
Передние центральные опухоли с поражением ЛМС и ППС (4, 5 и 8 сегменты) встречаются редко (4%). В этих условиях разработанные хирургические методики рекомендуют проводить центральную резекцию без трисекторэктомии.
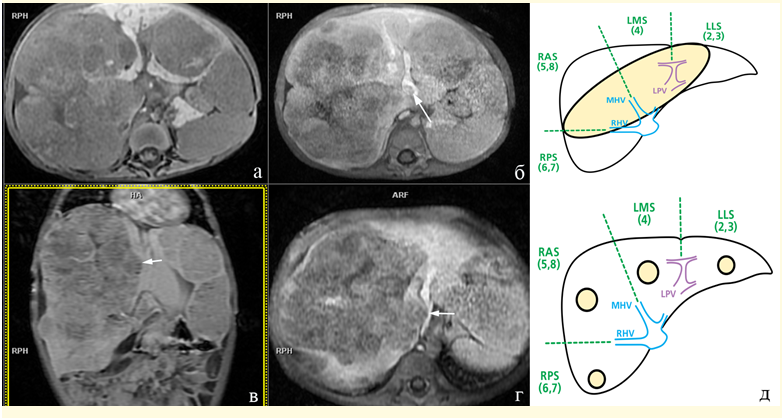
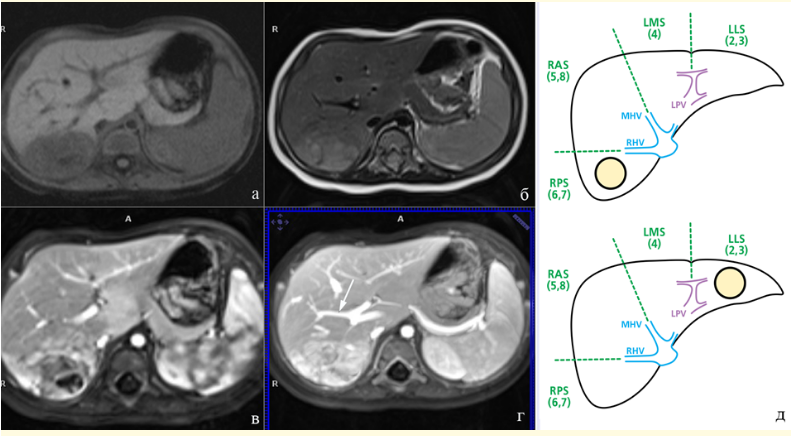
Рисунок 7.1.9. Пациент, 1 год 10 месяцев. Гепатобластома печени, РRETEXT IV. (а) – Т1 ВИ, мультифокальная форма ГБ; (б) - Т1 VIBE+КУ, тромб в устье левой вены печени (стрелка); (в, г) - Т1 VIBE+КУ, инвазия опухоли в нижнюю полую вену (НПВ) (короткие стрелки); (д) – схема топографии опухоли при PRETEX IV
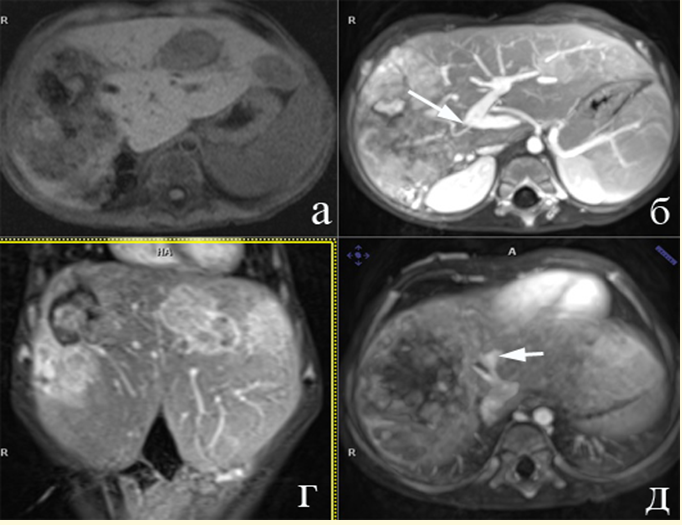
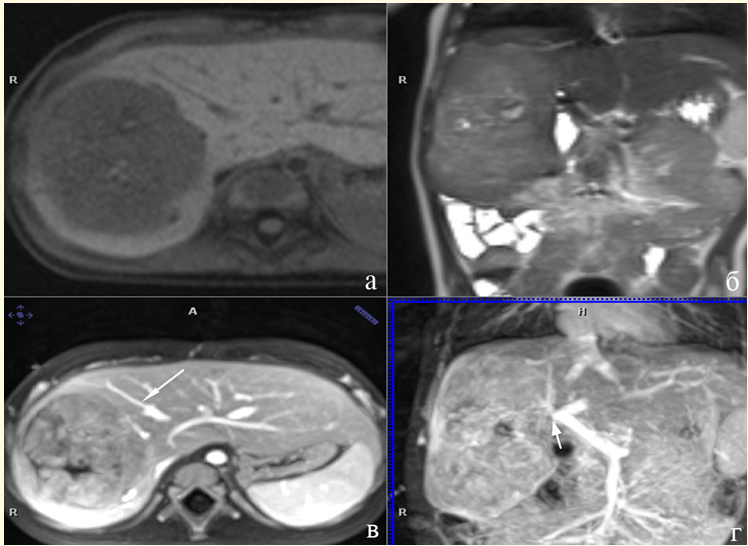
Рисунок 7.1.10. Пациент, 2 года. ГБ после курсов ПХТ, POSTTEXT IV. (а) - Т1 ВИ, уменьшение размеров образования; (б) Т1 VIBE+КУ инвазия ПВ ВВ (стрелка); (в) Т1 VIBE+КУ, множественные гиперваскулярные образования печени; (г) Т1 VIBE+КУ отсутствие тромба в левой вене печени (короткие стрелки).
Полученное по данным МРТ заключение o локализации опухолевых очагов и состояние афферентного/эфферентного кровотока, позволяет планировать у данной группы пациентов проведение предельно допустимых резекций печени с портальной и/или кавальной реконструкцией, билатеральные (билобарные) резекции или же выполнение трансплантации фрагмента печени.
Таблица стадирования по системе PRETEXT
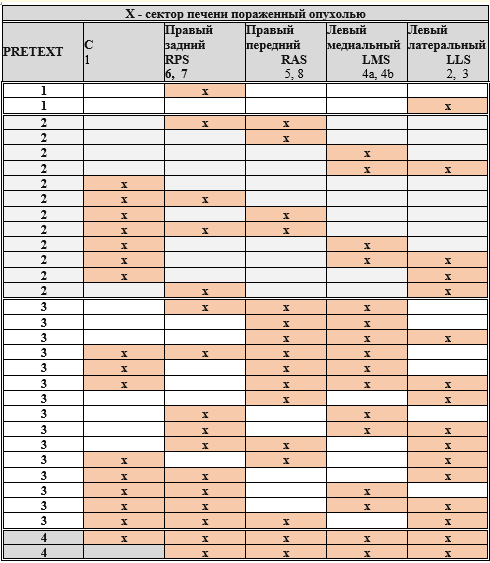
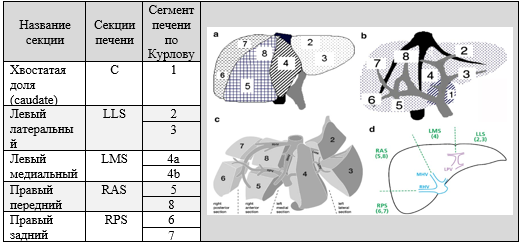
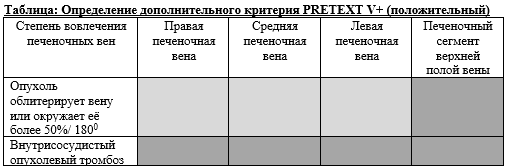
Критерии вовлечения в опухолевый процесс нижней полой вены SIOPEL: означает распространение в полую вену и/или в любую из трех печёночных вен
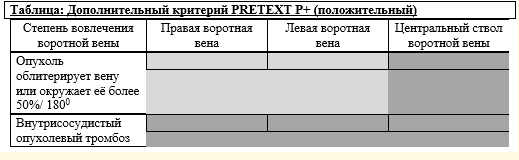
Считается положительным (P+ или P3+) если выбраны 2 светло-серых поля или любой из тёмно-серых.
Критерии вовлечения в опухолевый процесс портальной вены SIOPEL :
Степень распространения опухоли за пределы печени по системе PRETEXT*:
Комментарии: Рекомендовано заполнение таблицы для указания дополнительных критериев PRETEXT.
C
E
F
H
V
P
M
N
Критерий PRETEXT С – поражение первого сегмента печени (хвостатой доли)
*Несмотря на то, что только нижняя полая вена и главная воротная вена расположены за пределами печени, их главные притоки и ветви внутри печени также включаются в V и Р.
Примечание: V1+, V2+ и Р1+ = стандартный риск; V3+, Р2+ = высокий риск. Таким образом, определенная стадия по системе PRETEXT будет выражаться, например, как PRETEXT IV, V3+, Р1+, Е+, М+.
Расчет фактического объема опухоли не повлияет на окончательное распределение опухолей по четырем стадиям PRETEXT. Однако, расчет объема опухоли необходим для оценки возможного влияния на исход лечения пациента и для того, чтобы как можно точнее отследить ответ опухоли на терапию. Для упрощения вычислений «объем» будет означать фактическое произведение длин трёх максимальных перпендикулярных диаметров умноженное на коэффициент 0,52. Например: 112 мм х 98 мм х 119 мм х 0,52 = 679 мл (см3).
2. Патолого-анатомическое исследование опухолей печени
1. Гистологическое исследование.
Комментарии: Гистологическая классификация гепатобластомы принятая на консенсусе группы детской онкологии [53]:
2) Смешанные эпителиально-мезенхимальные варианты:
2. Описание гистологических вариантов
в) Плеоморфный низкодифференцированный компонент.
г) Эмбриональный компонент.
д) Мелкоклеточный недифференцированный компонент.
е) Смешанный эпителиальный. (присутствуют какие-либо/все вышеперечисленные компоненты).
ж) Эпителиальный холангиобластический компонент.
2.1 Смешанные эпителиально-мезенхимальные варианты;
б) Смешанная эпителиально-мезенхимальная ГБ с тератоидными характеристиками.
3. Иммуногистохимическое исследование.
Характеристика иммуногистохимических маркеров:
3. Рекомендации по хирургическому лечению
Биопсия проводится с целью забора достаточного количества опухолевого материала для:
Биопсия абсолютно* показана следующим группам пациентов:
Тонкоигольная биопсия не применяется, поскольку она не обеспечивает забора достаточного количества материала.
Технические аспекты
Предпочтительно выполнение собственно резекции печени при цифрах центрального венозного давления ниже 5 мм водного столба.
Радикализм и абластика во время резекции печени могут потребовать выполнения резекции как внутри- так и внепечёночных жёлчных протоков. Восстановление желчеотведения в подобных случаях должно осуществляться путём наложения билиодигестивного анастомоза (-ов) на выключенной по Ру петле тощей кишки.
В качестве дополнительного метода, улучшающего результаты хирургического лечения ГБ, может быть применена интраоперационная флуоресцентная визуализация с использованием индоцианина зеленого. При ее доступности, могут быть улучшены результаты вмешательств с сомнительной радикальностью по краю резекции и/или подозрением на внутрипеченочные метастазы малых размеров, а также в случаях необходимости хирургической эрадикации экстраорганных очагов (метастазы в лимфатические узлы и легкие). На сегодняшний день продемонстрирована эффективность и безопасность этого метода применительно к хирургии гепатобластомы [61, 62, 63, 64, 65].
ОТКАЗ от трансплантации в сторону резекции печени (включая билобарные) в случае исчезновения одного или нескольких очагов требует дальнейшего изучения и требует ОБЯЗАТЕЛЬНОГО информирования РОДИТЕЛЕЙ ребенка о достоверном ухудшении прогностических результатов трансплантаций, выполненных по поводу рецидива (трансплантация “второй линии”). Возможность выполнения трансплантации “второй линии” определяется совместным решением детских онкологов и трансплантологов с учетом первичного морфологического варианта опухоли, распространенности диагностированного рецидива, значений АФП (позитивный или негативный рецидив), химиочувствительности рецидивной опухоли. Рецидив опухоли после резекции не может рассматриваться в качестве абсолютного противопоказания к трансплантации.
Противопоказания к трансплантации печени:
При инициальном плохом ответе требуется пересмотр проводимого неоадъювантного протокола химиотерапии. При наличии признаков химиорезистентности опухоли (размеры очагов не уменьшаются или увеличиваются; имеются признаки повышения биологической активности опухоли в виде роста АФП) возможно выполнение трансплантации печени, как единственного метода спасения жизни пациента, с обязательным информированием родителей о плохом прогнозе результатов трансплантации. Выбор протокола адъювантной химиотерапии должен определяться с учетом химиорезистентности опухоли к инициальным препаратам и результатов морфологического и иммуногистохимического исследований.
Оптимальными сроками для трансплантации печени являются ближайшие 4 недели после окончания последнего курса химиотерапии.
Отсутствие вторичного поражения лёгких должно быть подтверждено современными методами визуализации.
4. Хирургическое лечение лёгочных метастазов
Технические аспекты
5. Лечебная тактика при наличии микроскопически определяемого остаточного заболевания
Когда все эти вопросы были рассмотрены, предлагаются следующие тактические решения:
2) Признаки того, что резецированный образец является частью мультифокальной гепатобластомы отсутствуют, и хирург знает, что осталось минимально измеряемое заболевание или микроскопические остаточные явления вдоль границ резекции. В этих случаях предполагается, что хирург должен промаркировать область остаточного заболевания и связаться с лучевыми терапевтами для решения вопроса о возможности проведения локальной лучевой терапии (stamp-like field).
3) Наличие признаков мультифокальной гепатобластомы не исключается. В этом случае предполагается, что уровень АФП не нормализуется. При отсутствии признаков внепеченочного заболевания должна быть рассмотрена возможность повторной хирургической операции. Ортотопическая трансплантация печени может рассматриваться в качестве метода выбора в подобной ситуации.
4. Оценка ответа на терапию
1. Критерии оценки ответа опухоли
Примечание:
2. Определение полной (хирургической) резекции
3. Определение полной ремиссии
Для того, чтобы сделать заключение о полной ремиссии, должны быть выполнены все следующие требования:
Примечание:
4. Критерии рецидива заболевания
Если наблюдается только повышенный уровень АФП без выявленных очагов опухолевого поражения, рекомендуется повторное определение уровня АФП. Если он продолжает возрастать, следует провести визуализационные исследования (УЗИ, КТ, МРТ, ПЭТ-сканирование, остеосцинтиграфия и т.д.) для поиска возможных сайтов локализации рецидива. Опыт показывает, что повышенный уровень АФП (биохимический рецидив) может регистрироваться за несколько недель до фактического обнаружения рецидива опухоли. Однако необходимо дождаться четкого определения локализации рецидива, чтобы обеспечить возможность проведения локального лечения.
5. Алгоритмы мониторинга состояния слуха на фоне терапии препаратами платины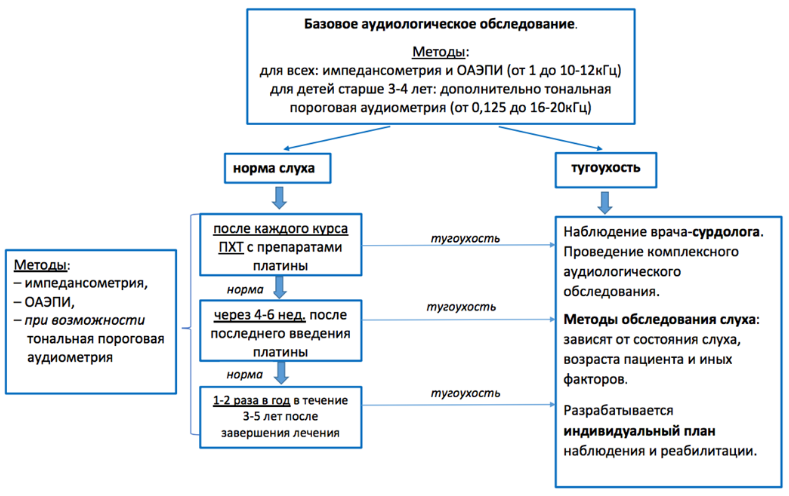
6. Правила пересчета результатов уровня АФП в различные единицы измерений.
Физиологические показатели АФП, обнаруженного в крови, находятся в пределах от 10 нг/мл до 8 МЕ/мл.
Для перерасчёта результатов нг/мл в МЕ/мл применяется формула: МЕ/мл * 1,21 = нг/мл; в случае обратного перевода значений МЕ/мл в нг/мл по формуле: нг/мл * 0,83 = МЕ/мл.
7. Референсные значения уровня АФП для детей первого года жизни [180]
Критерии оценки качества специализированной медицинской помощи детям при гепатобластоме (коды по МКБ - 10: С22.2)
Хирургническая и трансплантационная группа (в алфавитном порядке):
Лучевая диагностика:
Патоморфологическая диагностика:
Группа сопроводительной терапии (в алфавитном порядке):
Приложение А2. Методология разработки клинических рекомендаций
Таблица A2.1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица A2.2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
Таблица A2.3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций.
Таблица 1. Модификация доз химиопрепаратов в зависимости от массы тела [10, 67].
Приложение А3.2. Мониторинг состояния пациента при проведении химиотерапии.
Если необходима отсрочка на одну неделю и более, то в следующем курсе следует уменьшить дозу на 25% и использовать Г-КСФ.
Перед началом проведения химиотерапии:
Мониторинг ответа опухоли на химиотерапию:
Мониторинг токсичности химиотерапии:
Обследование перед операцией:
Для оценки ответа опухоли и ее размера:
В конце терапии:
Оценка опухолевого статуса:
Мониторинг токсичности химиотерапии на момент завершения:
Приложение А3.4. Рекомендации по введению лекарственных препаратов [68].
Инфузия #цисплатина**
Гидратация после введения #цисплатина** включает в себя не менее чем 12-часовую инфузионную терапию в дозе 3 л/м2 растворами 5% #декстрозы** и 0,9% раствора натрия хлорида**. Обязательным является добавление в инфузионные растворы электролитов:
Обратите внимание, что младенцы подвержены большему риску электролитного дисбаланса, вызванного #цисплатином** и, соответственно, необходимость регулярного контроля количества электролитов особенно важна для этой возрастной группы. Не забудьте также рассчитать количество восполняемой жидкости в соответствии с весом и возрастом младенца.
Приложение Б. Алгоритмы действий врача
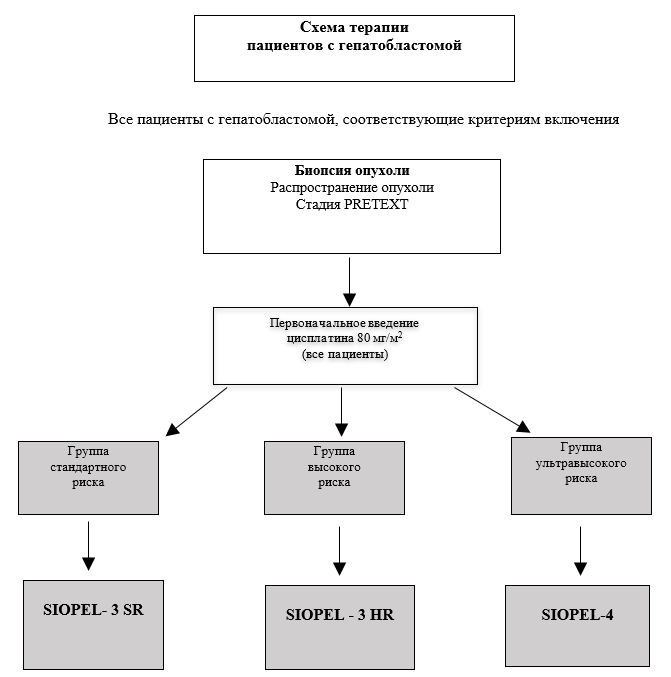
Алгоритм лечения пациентов с гепатобластомой группы стандартного риска
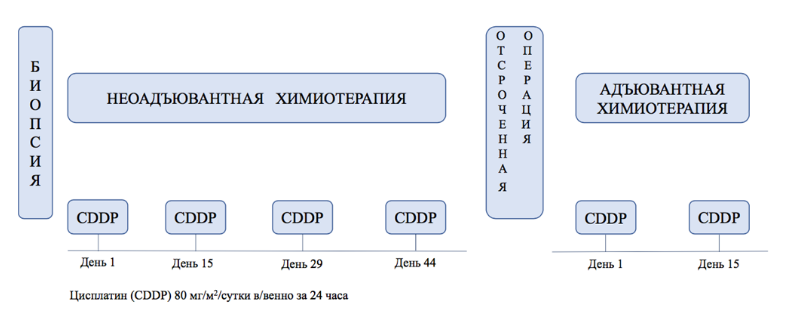
Алгоритм лечения пациентов с гепатобластомой группы высокого риска [10].
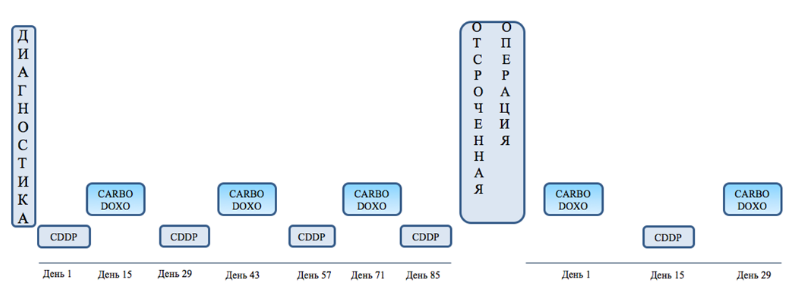
Алгоритмы лечения пациентов с гепатобластомой группы очень высокого риска.
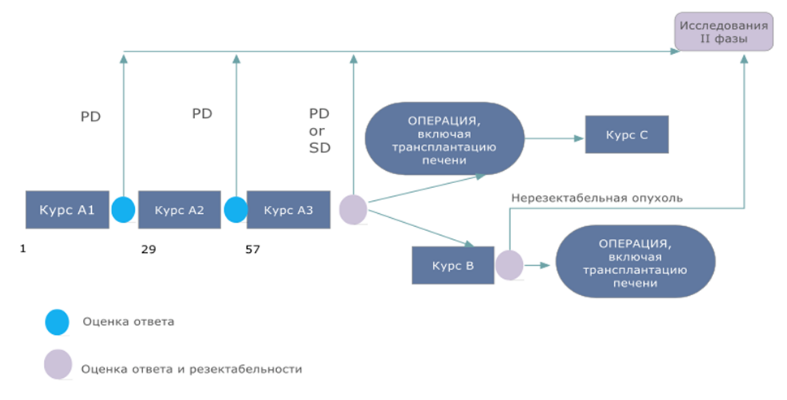
Что такое гепатобластома?
Причины возникновения гепатобластомы
Симптомы гепатобластомы
Крайне редко, когда опухолевые ткани продуцируют гормон – хорионический гонадотропин (именуемый гормоном беременности), у ребенка может наблюдаться преждевременное половое созревание.
Определение группы риска у пациентов позволяет выбрать оптимально достаточный объем терапии. Так, например, для группы очень низкого риска возможно излечение пациента только с помощь операции, а для пациентов группы очень высокого риска требуется высокоинтенсивная химиотерапия и, в ряде случаев, трансплантация печени.
Прикреплённые файлы
Внимание!
