Апластическая анемия у детей
Апластическая анемия у детей
 Версия: Клинические рекомендации РФ 2024 (Россия)
Версия: Клинические рекомендации РФ 2024 (Россия)
Общая информация
Краткое описание
Разработчик клинической рекомендации
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Выделяют следующие критерии тяжести приобретенной АА:
Сверхтяжелая апластическая анемия:
Тяжелая апластическая анемия
Нетяжелая приобретенная апластическая анемия
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Костномозговая недостаточность при АА развивается в результате подавления пролиферации гемопоэтических клеток-предшественниц активированными Т-лимфоцитами. Активация Т-лимфоцитов, экспансия цитотоксических Т-клонов и выброс медиаторов иммунной супрессии кроветворения (интерферон γ (ИФНγ), фактор некроза опухолей α) или стимулирующих пролиферацию и активацию Т-лимфоцитов (интерлейкин 2), приводят к нарушению процессов пролиферации и к стимуляции апоптоза клеток-предшественниц, вследствие чего происходит значительное уменьшение пула гемопоэтических клеток и развитие аплазии костного мозга [1–3].
Кроме того, течение АА может осложниться развитием таких клональных заболеваний как пароксизмальная ночная гемоглобинурия (ПНГ), миелодиспластический синдром (МДС), острый миелобластный лейкоз (ОМЛ). Частота развития клональных осложнений может достигать 32% в течение 10 лет [3,4]. Появление клонального кроветворения может быть выявлено и на более ранних этапах течения АА. В первую очередь речь идет об АА, протекающей с ПНГ-клоном [5,6]. При этом выявление клона с дефицитом гликозилфосфатидилинозитол (ГФИ) белков не означает развитие ПНГ как самостоятельного заболевания с картиной классического внутрисосудистого гемолиза. Размер ПНГ-клона в процессе течения АА может меняться до полного исчезновения [7]. Эволюция в классическую ПНГ, по данным различных авторов, составляет 11-17% [8–10].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
1. Жалобы и анамнез
2. Физикальное обследование
3. Лабораторные диагностические исследования
4. Инструментальные диагностические исследования
5. Иные диагностические исследования
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
2. Комбинированная иммуносупрессивная терапия в качестве первой линии патогенетической терапии АА
3. Терапия рефрактерных форм и рецидивов АА
4. Сопроводительное лечение пациентов с АА.
ов и/или антибиотиков гликопептидной структуры, в зависимости от клинической картины, локальных рекомендаций и колонизации пациента [119,121-123,138,141-144].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Госпитализация
Организация оказания медицинской помощи
Показания для экстренной госпитализации:
Показания к выписке пациента из стационара:
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Информация
Источники и литература
Информация
Термины и определения
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций.
1. Общие положения
3. Выбор донора и источника ГСК [50]
Донором для пациента с ПАА может быть:
Источник ГСК выбирается исходя из технологической платформы ТГСК, реализуемой в клинике. Источником ТГСК может являться:
4. Обследование пациента перед ТГСК [51]
Методы клинической лабораторной диагностики, применяемые при обследовании пациента перед ТГСК:
Инструментальные методы, применяемые при обследовании пациента перед ТГСК:
Консультации врачей-специалистов в предтрансплантационном периоде:
5. Обследование донора перед ТГСК [52]
Инструментальные методы, применяемые при обследовании донора перед ТГСК:
6. Заготовка трансплантата [53]
Подготовка донора
При использовании в качестве источника ГСК подготовка донора включает:
Заготовка трансплантата
Медикаменты и средства медицинского применения, необходимые для заготовки КМ донора:
Заготовка донорских СКПК [55]
Медикаменты и средства медицинского применения, необходимые для заготовки СКПК донора:
Заготовка ПК [56]
Обработка трансплантата ГСК [57]
Выбор метода (комбинации методов) обработки трансплантата определяется исходными характеристиками пары донор-реципиент, источником ГСК и технологической платформой ТГСК, реализуемой в трансплантационном центре.
Обязательными параметрами трансплантата ГСК, подлежащими контролю и регистрации, являются:
Дополнительными параметрами трансплантата ГСК, подлежащими контролю и регистрации, являются
Транспортировка и хранение трансплантата ГСК
7. Режим кондиционирования [59]
8. Введение в РТПХ [64]
3) «Синдром перекреста» оРТПХ и хРТПХ: сочетание типичных клинических проявлений оРТПХ и хРТПХ, независимо от срока развития.
4) хРТПХ: хроническое иммуно-опосредованное повреждение органов и тканей, в основе которого лежит нарушение формирования иммунологической толерантности. Гистопатологически характерен исход в фиброз.
9. Профилактика РТПХ
10. Приживление трансплантата (миелореконституция) [4]
11. Диагностика и терапия острой РТПХ [75]
При установлении клинического диагноза оРТПХ инициируется терапия, состав которой определяется тяжестью оРТПХ. Тяжесть оРТПХ и ответ на терапию первой линии определяют прогноз течения оРТПХ и выживаемости. При отсутствии ответа на терапию первой линии, принимают решение о назначении терапии второй и последующих линий.
Методы клинической лабораторной диагностики, применяемые при диагностике и терапии РТПХ [75]:
Инструментальные методы и пособия, применяемые при диагностике и терапии РТПХ [75]:
Медикаменты, используемые в терапии РТПХ (суточная доза) [75–77,87,164]:
12. Диагностика и терапия хронической РТПХ [87]
Тяжесть хРТПХ определяется на основании числа пораженных органов и степени выраженности нарушения функции пораженного органа (см. табл. 4) [89].
Примечания.
13. Профилактика и терапия инфекционных осложнений [90]
a. Бактериальные инфекции [91]
Профилактика бактериальных инфекций включает санитарно-эпидемические меры: контроль доступа, обработка рук персонала и ухаживающего члена семьи, микробиологическая безопасность продуктов питания и воды. Фармакологическая профилактика бактериальных инфекций возможна в соответствии с политикой инфекционного контроля в стационаре.
b. Вирусные инфекции [92]ваторно-синтициальный вирус. Вирусные инфекции у реципиентов ТГСК могут протекать в типичной форме, однако характерно тяжелое течение и генерализация инфекции.
Профилактика ВОБ включает выбор режима кондиционирования в соответствии с анализом факторов риска ВОБ, в частности отказ от применения высоких доз бусульфана** и комбинации алкилирующих средств у пациентов с предсуществующим поражением печени. Медикаменты, используемые в профилактике и терапии ВОБ суммированы ниже.
c. Мукозит [98]
d. Синдром задней обратимой энцефалопатии (PRES) [99]
15. Нутритивная поддержка [102]
16. Гемотрансфузионная терапия [103]
Донор и реципиент могут быть несовместимы по различным системам антигенов группы крови. В зависимости от характера несовместимости по системе АВ0 выделяют большая (major), малая (minor) и смешанная (major+minor). Под большой (major) несовместимостью по АВ0 системе подразумевают наличие в плазме у реципиента агглютининов, активных в отношении донорских эритроцитов, например при проведении ТГСК от донора с А(II) группой крови пациенту с 0(I) группой. Малая (minor) несовместимость по АВ0 системе обусловлена обратной ситуацией, то есть наличием в плазме донора ГСК агглютининов, активных в отношении эритроцитов реципиента, например при ТГСК от донора с 0(I) группой крови реципиенту с А(II) группой. О смешанной (major+minor) несовместимости говорят в том случае, когда и у донора, и у реципиента присутствуют агглютинины, активные в отношении эритроцитов реципиента и донора соответственно. В связи с вероятностью развития тяжелых осложнений, связанных с групповой АВ0-несовместимостью донора и реципиента ГСК, сформулированы правила проведения трансфузионной терапии после трансплантации (начиная с дня миелоинфузии), таблица 5.
Таблица 5. Правила проведения трансфузионной терапии у пациентов после ТГСК
Профилактика посттрансфузионной реакции трансплантат-против-хозяина.
Приложение Б. Алгоритмы действий врача
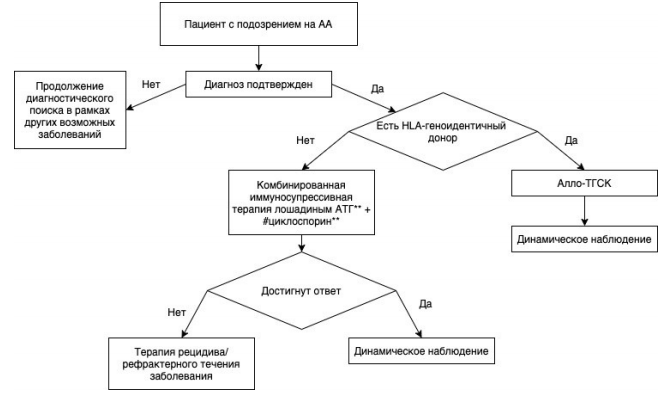
Апластическая анемия бывает разной степени тяжести: различают легкую, средней тяжести, тяжелую и сверхтяжелую формы АА.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Прикреплённые файлы
Внимание!
